Investigadores do Instituto Holandês do Cancro descobriram um novo mecanismo de morte de células cancerígenas envolvendo o gene Schlafen11, que poderá revolucionar a compreensão e o tratamento do cancro. Este gene ajuda a interromper a produção de proteínas em resposta a danos no ADN, oferecendo um novo alvo para terapias contra o cancro, especialmente nos casos em que as vias tradicionais da proteína p53 são ineficazes. Crédito: SciTechDaily.com
Os cientistas descobriram que a forma como as células cancerígenas morrem devido à quimioterapia parece ser diferente do que se entendia anteriormente. Novas pesquisas destacam o papel do gene Schlafen11 na morte das células cancerígenas, proporcionando uma nova abordagem às estratégias de quimioterapia e tratamento do câncer.
A quimioterapia mata células cancerígenas. Mas a forma como estas células morrem parece ser diferente do que se entendia anteriormente. Pesquisadores do Instituto Holandês do Câncer, liderados por Thijn Brummelkamp, descobriram uma forma completamente nova de morte das células cancerígenas: devido ao gene Schlafen11. “Esta é uma descoberta muito inesperada. Pacientes com câncer têm sido tratados com quimioterapia há quase um século, mas esse caminho para a morte celular nunca foi observado antes. Onde e quando isso ocorre nos pacientes precisará ser mais investigado. Esta descoberta poderia, em última análise, ter implicações para o tratamento de pacientes com câncer”. Eles publicaram suas descobertas na revista Ciência.
O papel dos danos ao DNA no tratamento do câncer
Muitos tratamentos contra o câncer danificam as células ADN. Depois de muitos danos irreparáveis, as células podem iniciar a sua própria morte. A biologia do ensino médio nos ensina que a proteína p53 se encarrega desse processo. A p53 garante a reparação do DNA danificado, mas inicia o suicídio celular quando o dano se torna muito grave. Isso evita a divisão celular descontrolada e a formação de câncer.
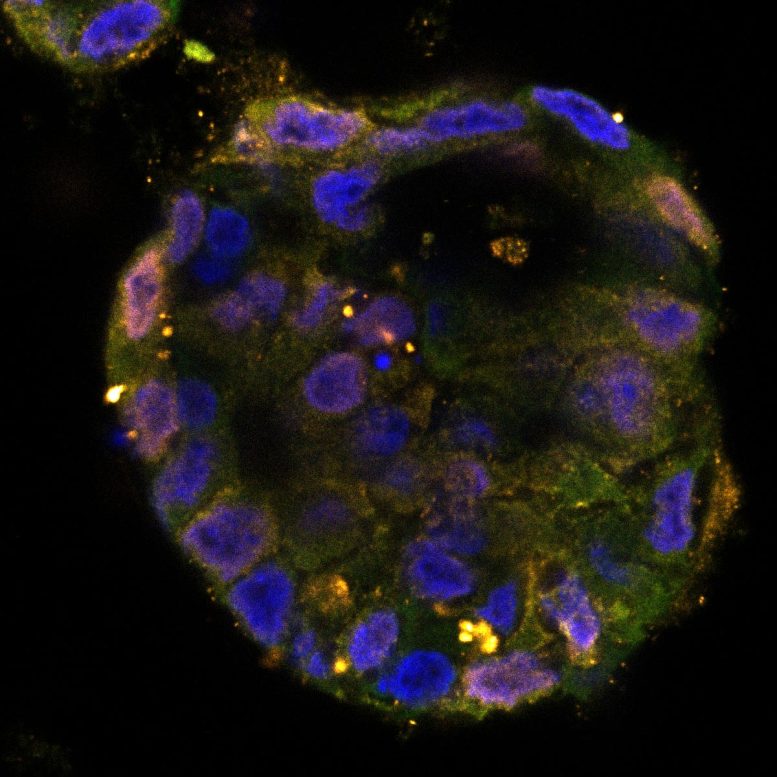
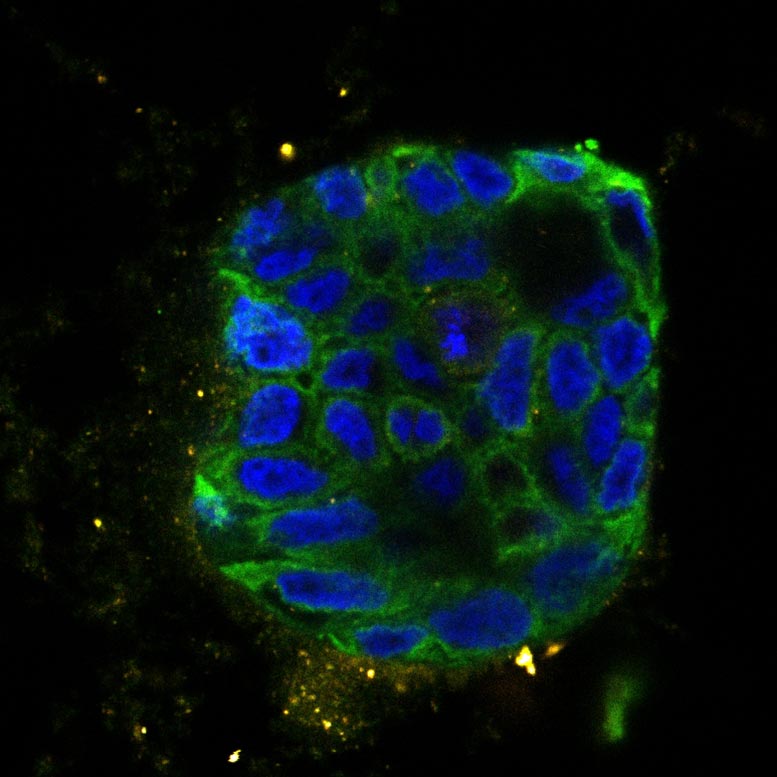
Organoide de paciente com câncer de cólon, tratado (inferior) e não tratado com quimioterapia etoposídeo. O tratamento causa danos ao DNA e redução na síntese de proteínas. Isso desencadeia um sinal de estresse que faz com que as células morram. Laranja: marcador de dano ao DNA. Verde: marcador para síntese protéica. Crédito: Instituto Holandês do Câncer
Surpresa: pergunta sem resposta
Parece um sistema infalível, mas a realidade é mais complexa. “Em mais da metade dos tumores, o p53 não funciona mais”, diz Thijn Brummelkamp. “O jogador-chave p53 não desempenha nenhum papel nisso. Então, por que as células cancerígenas sem p53 ainda morrem quando seu DNA é danificado com quimioterapia ou radiação? Para minha surpresa, essa era uma pergunta sem resposta.”
Seu grupo de pesquisa descobriu então, junto com o grupo do colega Reuven Agami, uma forma até então desconhecida pela qual as células morrem após danos no DNA. No laboratório, eles administraram quimioterapia em células nas quais modificaram cuidadosamente o DNA. Thijn: “Estávamos procurando uma mudança genética que permitisse às células sobreviver à quimioterapia. Nosso grupo tem muita experiência em desabilitar genes seletivamente, o que poderíamos perfeitamente aplicar aqui.”
Desligando genes, um por um
As pessoas têm milhares de genes, muitos dos quais têm funções que não são claras para nós. Para determinar o papel dos nossos genes, o pesquisador Thijn Brummelkamp desenvolveu um método usando células haplóides. Estas células contêm apenas uma cópia de cada gene, ao contrário das células normais do nosso corpo que contêm duas cópias. O manuseio de duas cópias pode ser um desafio em experimentos genéticos, porque muitas vezes ocorrem alterações (mutações) em apenas uma delas. Isto torna difícil observar os efeitos dessas mutações.
Juntamente com outros investigadores, Brummelkamp tem desvendado processos que são cruciais nas doenças há anos, utilizando este método versátil. Por exemplo, o seu grupo descobriu recentemente que as células podem produzir lipídios de uma maneira diferente do que anteriormente conhecido. Eles descobriram como certos vírus, incluindo o mortal Ebola vírus, conseguem entrar nas células humanas. Eles investigaram a resistência das células cancerosas contra terapias específicas e identificaram proteínas que atuam como freios no sistema imunológico, o que é relevante para a imunoterapia contra o câncer. Nos últimos anos, a sua equipa descobriu duas enzimas que permaneceram desconhecidas durante quatro décadas e que se revelaram vitais para a função muscular e o desenvolvimento do cérebro.
Novo ator-chave na morte celular
Ao desligar genes, o grupo de pesquisa encontrou um novo caminho para a morte celular liderado pelo gene Schlafen11 (SLFN11). O investigador principal Nicolaas Boon: “No caso de danos no DNA, o SLFN11 desliga as fábricas de proteínas das células: os ribossomos. Isso causa um estresse imenso nessas células, o que leva à sua morte. A nova rota que descobrimos contorna completamente a p53.”
O gene SLFN11 não é desconhecido na pesquisa do câncer. Muitas vezes é inativo em tumores de pacientes que não respondem à quimioterapia, diz Thijn. “Agora podemos explicar esta ligação. Quando as células não possuem SLFN11, elas não morrerão dessa maneira em resposta a danos no DNA. As células sobreviverão e o câncer persistirá.”
Impacto no tratamento do câncer
“Esta descoberta revela muitas novas questões de investigação, o que normalmente é o caso na investigação fundamental”, diz Thijn. “Demonstrámos a nossa descoberta em células cancerígenas cultivadas em laboratório, mas permanecem muitas questões importantes: onde e quando esta via ocorre nos pacientes? Como isso afeta a imunoterapia ou quimioterapia? Isso afeta os efeitos colaterais da terapia contra o câncer? Se esta forma de morte celular também desempenhar um papel significativo nos pacientes, esta descoberta terá implicações para os tratamentos do cancro. Estas são questões importantes para investigar mais profundamente.”
Referência: “Danos no DNA induzem apoptose independente de p53 por meio da paralisação do ribossomo” 16 de maio de 2024, Ciência.
DOI: 10.1126/science.adh7950
Esta pesquisa foi apoiada financeiramente pela KWF Dutch Cancer Society, Oncode Institute e Health Holland.